Introdução
A vitamina A (Retinol) e E (Tocoferol) têm papéis importantes nas funções fisiológicas para manter uma boa saúde. Publicações científicas relatam sua potencial implicação em diferentes patogêneses causadas pelo estresse oxidativo. Seu papel como biomarcadores é avaliado. Para grandes estudos epidemiológicos, técnicas analíticas precisas e de alto rendimento são necessárias.
Nosso objetivo para esta nota de aplicação é utilizar um método automatizado de preparação de amostra para a quantificação de vitamina A e E no soro usando uma única operação em LDTD-MS/MS.
O LDTD-MS/MS oferece especificidade combinada com uma análise ultrarrápida para um método de quantificação incomparável. Para desenvolver esta aplicação, nos concentramos em realizar uma preparação de amostra rápida e simples. As vitaminas A e E foram analisadas e os resultados foram obtidos em menos de 8 segundos por amostra.
Método de Preparação da Amostra
Extração automatizada de amostras
Devido à instabilidade das vitaminas A e E, as soluções estoque foram preparadas em etanol (0,1% BHT). O soro agrupado foi exposto à luz ultravioleta por pelo menos 24 horas para fotodegradar a vitamina endógena. O soro exposto reunido foi então adicionado para gerar uma curva de calibração e CQs.
As amostras foram transferidas para tubos com código de barras, legíveis pelo sistema de extração Azeo. Cada frasco com código de barras foi escaneado pelo Azeo Liquid Handler e um arquivo de lote automático foi criado. O sistema de extração Azeo (Figura 1) foi utilizado para extrair as amostras usando as seguintes condições:
- 5 µL de padrão interno (Retinol-d5 e Tocoferol-d6 a 10 mg/mL em EtOH (0,1% BHT)) foram adicionados a cada amostra
- 25 µL de amostra de soro foram transferidos dos frascos para uma placa de poços fundos colocada no Lumo Vortexer
- Misturados por 30 segundos a 1000 rpm
- 25 µL de tampão de extração (0,25 mM NaOH em Isopropanol: Água / 3,5:7,5) foram adicionados a uma placa de poço fundo
- Misturados por 30 segundos a 1000 rpm
- 300 µL de Hexano foram adicionados em uma placa de poço fundo
- Misturados por 5 minutos a 1000 rpm
- Houve uma pausa de 5 minutos para separação de fases
- Foram adicionados 6 µL da fase da camada superior em uma placa de 96 poços LazWell™
- Secados por 1 minuto em temperatura ambiente com fluxo de ar.
- Foram adicionados 6 µL de hidroxitolueno butilado (BHT, 100 µg/mL em hexano) em uma placa de 96 poços LazWell™
- Secados por 1 minuto em temperatura ambiente com fluxo de ar.

Parâmetros LDTD®-MS/MS |
|||||||||||||||||||||||||||||||||||||||||||||||
| Shimadzu | Thermo | Sciex | |||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| LDTD
Modelo: Luxon SH-960, Phytronix Gás carreador: 9 L/min (ar) Padrão de laser:
MS/MS Modelo MS: LCMS-8060, Shimadzu Tempo de escaneamento: 50 milissegundos Tempo total de execução: 8 segundos por amostra Ionização: APCI Método de análise: Modo MRM positivo |
LDTD
Modelo: Luxon T-960, Phytronix Gás carreador: 9 L/min (ar) Padrão de laser:
MS/MS Modelo MS: Thermo Vantage, Thermo Fisher Scientific Tempo de escaneamento: 50 milissegundos Tempo total de execução: 6 segundos por amostra Ionização: APCI Método de análise: Modo MRM positivo |
LDTD
Modelo: Luxon S-960, Phytronix Gás carreador: 9 L/min (ar) Padrão de laser:
MS/MS Modelo MS: Q-Trap System® 5500, Sciex Tempo de escaneamento: 40 milissegundos Cortina: 30 Tempo total de execução: 8 segundos por amostra Ionização: APCI Método de análise: Modo MRM positivo |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Tabela 1 – Transições MRM para LDTD-MS/MS |
|||||||||||||||||||||||||||||||||||||||||||||||
| Shimadzu | Thermo | Sciex | |||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
As seções a seguir foram retiradas da nota de aplicação 2107B para o espectrômetro de massa da Shimadzu. Para todas as aplicações de: « Análises de vitamina A e E no soro como biomarcadores de distúrbios clínicos » (Shimadzu, Thermo e Sciex), baixe o PDF anexado a este artigo.
Resultados e Discussão
Processo de preparação de dados
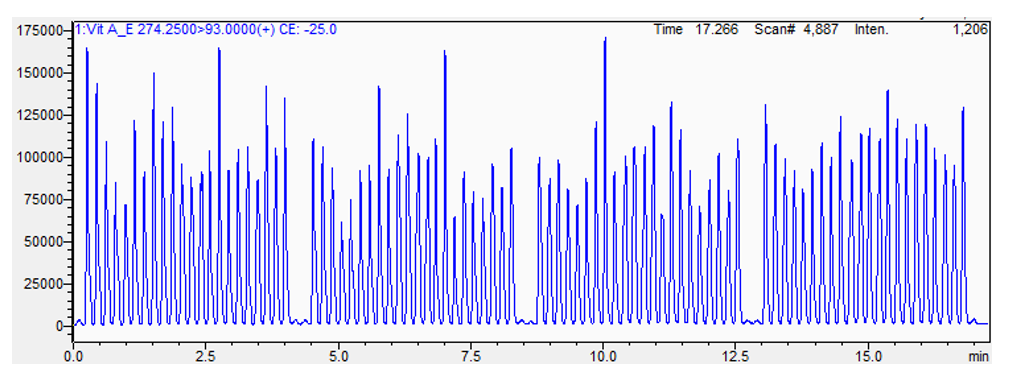
Espectrômetros de massa são sistemas de aquisição de dados que não foram projetados para lidar com poucos segundos de sinal por amostra. A sequência de sincronização adiciona de 6 a mais de 15 segundos entre cada amostra. Para contornar isso, todas as amostras são adquiridas em um único arquivo (Figura 2). Para permitir a análise desses dados, o software Cascade foi projetado para detectar, dividir e integrar cada pico de amostra adquirido em um único arquivo.
Teste de validação
Curvas de calibração variando de 191 a 2191 ng/mL para Retinol e de 3,1 a 43,1 mg/mL para Tocoferol foram preparadas em soro exposto à luz ultravioleta. Três amostras de soro humano foram usadas como CQ (os valores de concentração endógena foram avaliados com um método de referência e usados como valor nominal). Extrações replicadas foram depositadas em uma placa LazWell™ e secas antes da análise. A área do pico contra a razão do padrão interno (PI) foi usada para normalizar o sinal.
Linearidade
As curvas de calibração foram traçadas usando a razão da área do pico e a concentração nominal dos padrões. Para o teste de linearidade, o seguinte critério de aceitação foi utilizado:
- A regressão linear (r2) deve ser ≥ 0,99
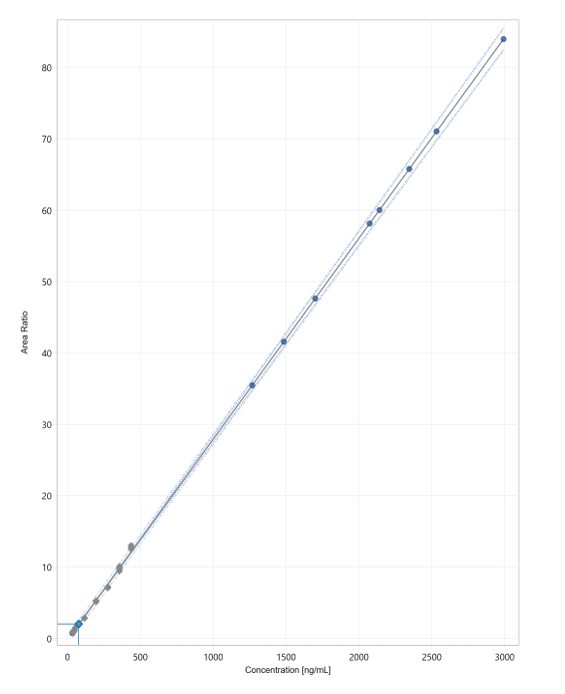
Figura 3 mostra um resultado típico da curva de calibração para Tocoferol. Resultados semelhantes foram obtidos para o Retinol.
Precisão e Exatidão
Para a avaliação da exatidão e precisão, foram utilizados os seguintes critérios de aceitação:
- Cada concentração não deveria exceder 15% CV.
- Cada concentração deveria estar dentro de 100 ± 15% da concentração nominal.
Para o experimento de precisão e exatidão entre corridas, cada CQ foi analisado em triplicata, em cinco dias diferentes. As Tabelas 2 e 3 mostram os resultados de precisão e exatidão entre corridas para Retinol e Tocoferol, respectivamente. O %CV obtido ficou abaixo de 15% e a exatidão ficou dentro de 15% do valor nominal.
Tabela 2 – Precisão e exatidão entre corridas do retinol
| Retinol | CQ-L | CQ-M | CQ-H |
|---|---|---|---|
| Conc (ng/ml) | 391 | 991 | 1791 |
| N | 15 | 15 | 15 |
| Média (ng/ml) | 405.0 | 942.2 | 1755.5 |
| SD | 23.1 | 63.4 | 118.8 |
| %CV | 5.7 | 6.7 | 6.8 |
| %Nom | 103.6 | 95.1 | 98.0 |
Tabela 3 – Precisão e exatidão entre corridas do Tocoferol
| Tocoferol | CQ-L | CQ-M | CQ-H |
|---|---|---|---|
| Conc (mg/ml) | 7.1 | 19.1 | 35.1 |
| N | 15 | 15 | 15 |
| Média (mg/ml) | 7.7 | 19.6 | 33.3 |
| SD | 0.8 | 1.0 | 0.7 |
| %CV | 10.4 | 5.1 | 2.3 |
| %Nom | 108.4 | 102.5 | 94.9 |
Estudo de validação cruzada
Amostras de soro de pacientes reais (N=6) foram testadas com este método para correlacionar com os resultados obtidos por LC-MS/MS tradicional. A porcentagem de diferença entre os valores foi avaliada. Obteve-se uma diferença inferior a 15%. Os resultados são relatados na Tabela 4.
Tabela 4 – Resultado de validação cruzada
| Vitamina A (retinol) | Vitamina E (tocoferol) | ||||||
|---|---|---|---|---|---|---|---|
| LC (ng/mL) |
Luxon (ng/mL) |
%Diff (%) |
LC (mg/mL) |
Luxo (mg/mL) |
%Diff (%) |
||
| M1 | 479 | 449 | -3.3 | 13.7 | 15.6 | 6.5 | |
| M2 | 411 | 423 | 1.4 | 10.0 | 11.1 | 5.3 | |
| M3 | 551 | 554 | 0.3 | 9.9 | 11.1 | 5.8 | |
| M4 | 581 | 538 | -3.8 | 15.2 | 17.7 | 7.5 | |
| M5 | 820 | 701 | -7.8 | 13.9 | 16.1 | 7.2 | |
| M6 | 553 | 609 | 4.7 | 10.8 | 12.2 | 6.0 | |
Conclusão
O Luxon Ion Source® combinado com o sistema de espectrometria de massa Shimadzu LCMS-8060 permite análises ultrarrápidas (8 segundos por amostra) de Vitamina A e E no soro.